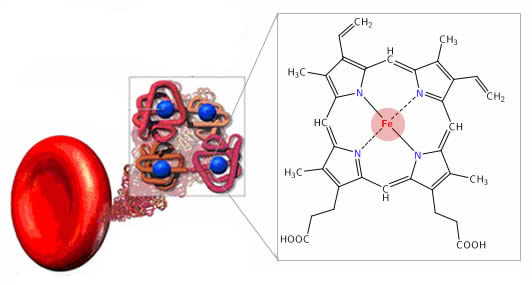
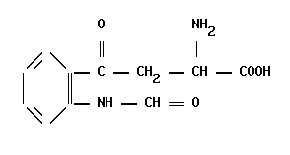
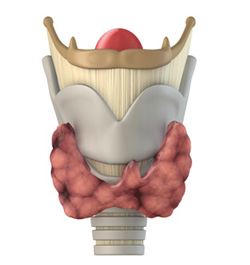
Классификация ядерных рецепторов и их лиганды
Природные высокоаффинные лиганды
Природные высокоаффинные лиганды PXR пока не выявлены. Возможно, ими являются метаболиты стероидов. Быть может, именно через PXR реализуются многие из известных побочных эффектов рифампицина. Например, длительная терапия рифампицином повышает скорость метаболического клиренса стероидов. Рифампицин быстро снижает уровень вводимых извне стероидов (например, у больных с болезнью Аддисона, принимающих кортикостероиды; у женщин, принимающих пероральные контрацептивы). Ортолог PXR у эмбрионов шпорцевой лягушки — BXR (Рц X бензоатов) связывает метаболиты бензоата (алкильные эфиры амино- и гидроксибензойной кислоты), возможно, участвующие в регуляции морфогенеза. Эти лиганды структурно сходны с ияра-аминобензойной кислотой, являющейся предшественником фолиевой кислоты и присутствующей в пище.
CAR. В отличие от большинства других Рц, лиганды конститутивно активных ядерных Рц CAR (андростанол, андростенол) не повышают, а снижают транскрипционную активность Рц, вызывая диссоциацию комплексов Рц с коактиватором. Это напоминает ситуацию с негативными HREs для ядерных Рц. Фенобарбитал и его аналоги, конкурируя с андростанами, восстанавливают активность CAR (в частности, в индукции генов семейства цитохромов Р450 2В). PXR, CAR, PPAR и некоторые другие ядерные Рц, по-видимому, могут участвовать в неспецифической адаптации организма по Селье за счёт проведения сигналов эндогенных и экзогенных лигандов («кататоксических соединений»), индуцирующих цитохромы Р450, которые защищают от последующего действия токсичных ксенобиотиков, а также стимуляции выведения ксенобиотиков с жёлчью.
HNF4. Ядерный фактор гепатоцитов HNF4a (hepatocyte nuclear factor) интенсивно экспрессируется в печени и ряде других органов, тогда как HNF4y (вопреки своему названию) в печени не обнаружен. Члены подгруппы в виде гомодимеров связываются с HREs в форме прямых повторов со спейсером из 1 п.н.
Мутации гена HNF4a
Такие HREs найдены во многих специфичных для печени генах, а также в генах, определяющих обмен углеводов, липидов и аминокислот. Лиганды HNF4a — ацил-КоА-тиоэфиры длинноцепочечных жирных кислот, причём поли- и мононенасыщенные ацил-КоА тормозят конститутивную активность Рц, а насыщенные — повышают (пальмитоил-КоА) или снижают (стеароил-КоА). Мутации гена HNF4a ассоциированы с неинсулинзависимым сахарным юношеским диабетом.
Нокаут гена у мышей приводит на 6,5 день развития к апоптозу клеток эктодермы, нарушениям дифференцировки мезодермы и гибели эмбрионов. Более позднее (на 8,5 день развития) повреждение гена ведёт к снижению экспрессии ферментов гликолиза и белков транспорта глюкозы и жирных кислот.
RXR. Рц X ретиноидов (RXRa.P,Y> активируются 9-г<«с-ретиное-вой кислотой и нециклическими терпеноидами — метопреном и фитановой кислотой. Фитановая кислота — продукт распада хлорофилла — содержится в пище, а метопрен — промышленный пол-лютант. RXR может действовать в виде гомодимеров RXR/RXR или гетеродимеров с другими ядерными Рц. Активация непермиссивных гетеродимеров может быть достигнута только в присутствии лиганда партнёра RXR [для димеров RAR/RXR, TR/ RXR, VDR/RXR (vitamin D receptor — Рц 1сх,25-дигидроксивита-мина D3)]. Активация пермиссивных димеров достигается в присутствии лигандов либо RXR, либо его партнёра. Разрушение гена RXRa приводит к дефектам морфогенеза плаценты, сердца, глаза, ведущим к гибели эмбрионов. Разрушение гена в гепатоцитах взрослых животных сопровождается многообразными нарушениями обменных процессов (в частности, обмена холестерина, экспрессии ряда цитохромов Р450), регуляторами которых служат димеры RXR с другими ядерными Рц (PPARa. CAR(3, PXR, LXR, FXR [фарнезоидов]), а также укорочением жизни гепатоцитов, особенно при регенерации и при возрастании плоидности клеток.
Разрушение гена RXRP
Разрушение гена RXRP сопровождается нарушениями сперматогенеза и преждевременным развитием альвеол лёгких, а при нокауте гена RXRy обнаружены различные нарушения развития холинергических нейронов в экстрапирамидных путях мозга, а также функций гиппокампа.
TR2. Рц семенников группы TR2 функционируют преимущественно как репрессоры транскрипции, взаимодействуя с ДНК в виде гомо- или TR2/TR4-reTepo;HiMepoB. Их HREs — прямые повторы, в которых размер спейсера может варьировать от 1 до 5 п.н. Зафиксировано также действие TR4 в форме мономера. Репрессорное действие включает прямое взаимодействие с гистондеацетилазами.
TLX. Особенностью гомолога гена tailless (TLX) является его предпочтительное взаимодействие с модифицированным HRE, в котором второй консенсусный G заменен на A. TLX экспрессируется преимущественно в развивающемся переднем мозге. Нокаут гена у мышей ведёт к недоразвитию обонятельных луковиц, миндалевидного тела, зубчатой извилины. Животные становятся чрезмерно агрессивными, а самки отказываются выхаживать свое потомство.
COUP-TF. Члены группы COUP-TF (chicken ovalbumin upstream promoter transcription factors — транскрипционный фактор отдалённого промотора овальбумина цыплят) выступают в роли транскрипционных репрессоров, тормозящих активирующее действие многих ядерных Рц. Они способны взаимодействовать со многими типами HRE (прямыми, обратными или вывернутыми повторами) в форме гомодимеров, а также в форме гетеродимеров с RXR. Выключение гена COUP-TFI ведёт к нарушениям развития периферической нервной системы у мышей, что сопровождается затруднениями в осуществлении сосания и глотания у новорождённых и гибели от истощения и дегидратации. Нокаут гена COUP-TFII приводит к гибели эмбрионов мышей на 10-й день развития из-за дефектов ангиогенеза и развития сердца.
Нарушения липидного обмена
ERs. Рц эстрогенов в некоторых отношениях являются пограничными между другими Рц стероидных гормонов и остальными ядерными Рц. ERs, как и другие Рц стероидов, взаимодействуют с белком теплового шока Hsp90, и их HREs организованы в виде палиндромов. Но по нуклеотидным последовательностям эти элементы близки к HREs для ядерных Рц, отличных от Рц стероидов.
ERR. Родственные Рц эстрогенов ERRs широко экспрессируются в организме. Они могут взаимодействовать с ДНК в виде мономеров и гомодимеров. В последнем случае ERR узнают эстроген-чувствительные элементы. Их транскрипционная активность регулируется некоторыми синтетическими аналогами эстрогенов и поллютантами. Эндогенные лиганды ERRs пока не идентифицированы. Нокаут гена ERRP ведёт к нарушению формирования плаценты и гибели эмбрионов мышей на 10,5 сутки развития. По предварительным данным, нокаут гена ERRa приводит к нарушениям липидного обмена, что коррелирует с преобладающей экспрессией этого Рц в тканях с интенсивным р-окислением жирных кислот.
GR, MR, PR, AR. Рц стероидных гормонов (глюкортикоидов — GR, минералокортикоидов — MR, прогестерона — PR и андрогенов — AR) обладают рядом отличий от других ядерных Рц. Они взаимодействуют с белком теплового шока Hsp90, экранирующим ДНК-связывающий домен Рц. Гормональный лиганд вызывает отделение Hsp90. Вторым важным отличием этой подгруппы Рц служит тип узнаваемых ими HREs — палиндромных структур, построенных из шестичленных полусайтов и разделенных спейсером из 3 п.н.
NGFI-B. Рц подсемейства NGFI-B (белок В, индуцируемый фактором роста нервов NGF) экспрессируются преимущественно в клетках нервной системы и составляют часть немедленного ответа на такие стимулы, как факторы роста и деполяризация. Эти Рц найдены также в гипофизе, надпочечниках, печени и ряде других органов. Взаимодействуют с ДНК как мономеры, гомо- и гетеро-димеры с PvXR.
Ядерная локализация
Ядерная локализация, связывание с ДНК и транскрипционная активность NGFI-B могут регулироваться фосфорилированием. Разрушение гена NGFI-B не влияет существенно на фенотип мышей, но выключение гена NURR1 (Рц 1, родственный ядерному Рц Nur77) приводит к гибели животных вскоре после рождения. У таких мышей не развиваются дофаминергические нейроны среднего мозга.
SF1. Стероидогенный фактор 1 экспрессируется преимущественно в стероидогенных тканях, а также в гипоталамусе и гипофизе. Это мономерный Рц, взаимодействующий с HREs ряда генов ферментов синтеза стероидных гормонов, АМН, ЛГ, Рц АКТГ. Его транскрипционная активность регулируется фосфорилированием (в частности, под действием гормональных стимулов — АКТГ, ЛГ, усиливающих образование цАМФ). Фосфорилирование домена AF-1 приводит к рекрутированию коактиватора SRC-2. Нокаут гена SF1 у мышей ведёт к агенезу гонад и надпочечников, нарушениям половой дифференцировки и гибели животных вскоре после рождения. Рентгеноструктурный анализ родственного SF1 Рц (LRH1) показал, что лигандсвязывающий карман в этих Рц не имеет входа. Поэтому весьма вероятно, что данные Рц не регулируются лиган-дами.
GCNF (germ cell nuclear factor — ядерный фактор зародышевых клеток) экспрессируется преимущественно в клетках ранних эмбрионов. Его выключение у мышей приводит к гибели эмбрионов. При этом наблюдается ряд дефектов органогенеза: нервная трубка остаётся открытой, снижено количество сомитов, развиваются эктопические точки роста хвоста при нарушении связи между хорионом и аллантоисом.
DAX-1, SHP. Рц DAX-1 (критическая область чувствительного к дозе обращения пола и наследуемой гипоплазии надпочечников хромосомы X) и SHP (малый партнёр гетеродимеризации) отличаются от других ядерных Рц отсутствием типичного ДНК-связываю-щего домена. DAX-1 узнаёт шпильковые структуры ДНК, a SHP не взаимодействует с ДНК. DAX-1 экспрессируется в гипоталамусе, гипофизе, надпочечниках и гонадах.
- Предыдущие статьи из рубрики: Эндокринология