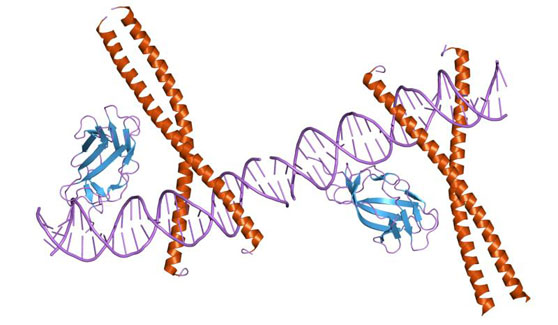
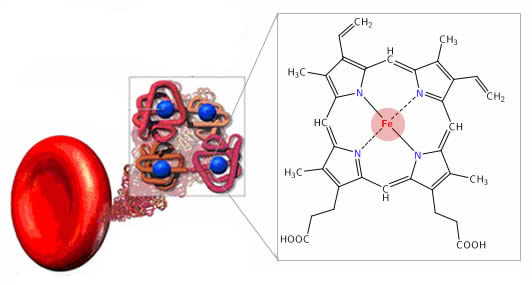
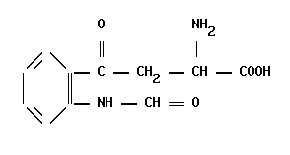
Рецепторы, сопряжённые с g-белками
Мутации гена SHP
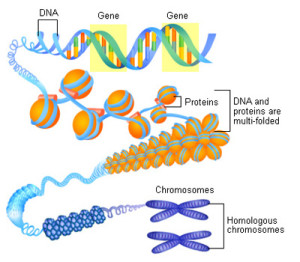 Совместно со стероидогенным фактором 1 (SF1) и продуктом гена SRY (sex determining region Y — детерминирующая пол область Y-хромосомы) DAX-1 определяет половую дифференцировку и развитие гонад и коры надпочечников. Может образовывать гетеродимеры с SF1, ингибируя при этом транскрипционную активность SF1. Самцы мышей с нокаутированным геном DAX-1 стерильны из-за нарушений дифференцировки и пролиферации клеток Ляйдига и Сертоли семенников. У 1/3 животных старше года развиваются опухоли репродуктивного тракта. SHP образует гетеродимеры со многими ядерными Рц, что ведёт к снижению их транскрипционной активности. Это осуществляется за счёт двух механизмов: торможения связывания Рц с ДНК и действия собственной репрессорной функции N-концевой области SHP. Мутации гена SHP ассоциированы с ожирением.
Совместно со стероидогенным фактором 1 (SF1) и продуктом гена SRY (sex determining region Y — детерминирующая пол область Y-хромосомы) DAX-1 определяет половую дифференцировку и развитие гонад и коры надпочечников. Может образовывать гетеродимеры с SF1, ингибируя при этом транскрипционную активность SF1. Самцы мышей с нокаутированным геном DAX-1 стерильны из-за нарушений дифференцировки и пролиферации клеток Ляйдига и Сертоли семенников. У 1/3 животных старше года развиваются опухоли репродуктивного тракта. SHP образует гетеродимеры со многими ядерными Рц, что ведёт к снижению их транскрипционной активности. Это осуществляется за счёт двух механизмов: торможения связывания Рц с ДНК и действия собственной репрессорной функции N-концевой области SHP. Мутации гена SHP ассоциированы с ожирением.
Данные Рц составляют самое большое надсемейство белков, в него входит более 1000 членов. Гены этих Рц составляют >1% генома человека. Лигандами этих Рц могут служить биогенные амины, пептиды, белки, липиды, нуклеотиды, ионы. Рц этого надсемейства опосредуют восприятие света, запаха и вкуса. Более того, вирус иммунодефицита человека использует Рц этого типа в качестве кофактора для проникновения в клетку. Из существующих лекарственных средств >50% специфичны в отношении данной группы Рц.
Структура и классификация рецепторов
Единственной общей чертой всех членов надсемейства является наличие 7 пронизывающих мембрану а-спиральных сегментов (ТМ), соединённых вне- и внутриклеточными петлями, причём N-конец молекулы обращен наружу, а С-конец — внутрь клетки. Эти трансмембранные сегменты (домены) расположены по замкнутому контуру, против часовой стрелки при виде извне клетки.
Лигандсвязывающие домены
Гомология выявляется внутри подсемейств этих Рц. Рц млекопитающих относятся к 3 семействам: А (родопсина, р2-АдРц), В (Рц глюкагона) и С (метаботропные Рц нейромедиаторов).
Для большинства членов семейства А характерно наличие остатка пальмитиновой кислоты, присоединённого к цистеинилу С-конца молекулы, что обеспечивает образование дополнительной внутриклеточной петли. Для членов семейства В характерен длинный (около 100 остатков) N-конец. Члены семейства С имеют очень длинный N-конец (около 600 остатков) и очень короткую 3-ю цитоплазматическую петлю.
В отличие от других Рц семейства, родопсин связывает свой лиганд — 11-г<ис-ретиналь — ковалентно. Связывающий карман формируется внешними частями ТМ 3, 6 и 7. Аналогичным образом карман связывания адреналина в (32-АдРц формируется ТМ 3, 5, 6 и 7, но этот карман расположен глубже, чем в родопсине. Особую роль здесь играет консервативный для подсемейства Aspll3 в ТМ 3, взаимодействующий с положительно заряженной аминогруппой биогенных аминов. Структурно несходные с агонистами антагонисты могут взаимодействовать с более поверхностно расположенными остатками, включая остатки внеклеточных петель. Карман связывания эйкозаноидов также расположен в щели, образуемой ТМ. В Рц семейства А для пептидных регуляторов в связывании лигандов (помимо ТМ) первостепенное значение имеют внеклеточные домены, причём даже в близкородственных Рц вклад трансмембранных и внеклеточных доменов различен. Низкомолекулярные аналоги пептидов могут взаимодействовать с иными остатками, часто локализованными в щели между ТМ. Димерные гликопротеидные гормоны типа ЛГ взаимодействуют с Рц, по-видимому, в два этапа: сначала они связываются с длинным N-концом рецепторной молекулы, претерпевают конформационную перестройку и взаимодействуют затем с внеклеточными петлями Рц. Рц тромбина активируется особым образом: тромбин отщепляет 33-членный N-концевой фрагмент Рц, который выступает далее в качестве лиганда того же Рц, взаимодействуя с его внеклеточными петлями.
Параметры лигандрецепторного взаимодействия
В связывании лигандов Рц семейств В и С ключевую роль играет длинный N-концевой фрагмент, а также (семейство В) внеклеточные петли Рц.
Параметры лигандрецепторного взаимодействия могут быть объектом разнообразных регуляторных влияний. В частности, обнаружен класс мембранных белков, модифицирующих активность Рц (RAMPs — receptor activity modifying proteins), взаимодействующих с Рц, подобным Рц кальцитонина (CRLR — calcitonin receptorlike receptor). Эти белки, во-первых, направляют Рц в плазматическую мембрану (т.е. выполняют функцию шаперонов), и, во-вторых, меняют лигандную специфичность Рц: RAMP1 обеспечивает предпочтительное взаимодействие Рц с пептидом, относящемся к гену кальцитонина (CGRP), a RAMP2 — с адреномедуллином.
Механизмы активации рецепторов
По-видимому, существует множество путей активации Рц. Об этом свидетельствует обнаружение активирующих Рц AT против фрагментов внеклеточных петель otj и Pj-АдРц (у больных со злокачественной гипертензией и идиопатической дилатационной карди-омиопатией), мускариновых Рц и Рц В2 брадикинина, а также ауто-антител против внеклеточных доменов Рц ТТГ при болезни Грейвса.
Многие Рц обладают базальной активностью, т.е. способны активировать G-белки в отсутствие агониста. Эта конститутивная активность может значительно усиливаться под действием ряда активирующих мутаций Рц, которые могут быть приурочены практически ко всем доменам Рц. В частности, обнаружены активирующие мутации во 2-й внеклеточной петле Рц ТТГ, в 3-й внеклеточной петле Рц тромбина. Подобные мутации ассоциированы с наследственными заболеваниями (например, наследуемыми аденомами щитовидной железы в случае мутации Рц ТТГ, преждевременным половым созреванием при мутации Рц ЛГ и т.д.).
Внутримолекулярные взаимодействия
Замена А1а293 3-й внутриклеточной петли ос1Ь-АдРц на любую другую аминокислоту повышает конститутивную активность Рц. Это позволило предположить, что в Рц имеют место внутримолекулярные взаимодействия, сдерживающие конститутивную активность, а лиганд или активирующая мутация снимают эти взаимодействия. В ряде Рц такую сдерживающую функцию выполняет ТМ 6. В случае представителей семейства А предполагается, что снятие тормозных взаимодействий в Рц под действием агониста в качестве ключевого момента включает протонирование аспарагиновой кислоты в консервативном мотиве Glu/Asp-Arg-Tyr цитоплазматической части ТМ 3. Это сопровождается значительными изменениями конформации всей рецепторной молекулы (в частности, перемещениями ТМ 3, 6 и 7), возможно, за счёт образования новой связи соседнего с Asp Arg с Asp ТМ 2.
Во взаимодействии с G-белками ведущую роль играют 2-я и 3-я цитоплазматические цепи Рц, а в некоторых случаях — и проксимальная часть С-конца рецепторной молекулы. Специфичность Рц по отношению к определённым ос-СЕ G-белков придают примембранные части 3-й цитоплазматической петли. 2-я цитоплазматическая петля служит своего рода выключателем, определяющим возможность взаимодействия Рц с G-белком. Подробности взаимодействия Рц с G-белками остаются неизвестными. Полагают, что центр связывания нуклеотидов в а-СЕ G-белков регулируется Рц аллостерически.
Для многих сопряжённых с G-белками Рц показано образование гомодимеров. Механизмы димеризации разных Рц могут различаться, с преобладанием взаимодействий трансмембранных сегментов (в р2-АдРц), С-концевых областей (в Рц 5 опиоидов) или образования дисульфидных связей N-концевых доменов (в метаботропных Рц глутамата). Агонист стабилизирует димеры Рц. По-видимому, димеризация может быть непосредственно связана с активацией Рц: только бивалентные AT против Рц хемокинов CCR2b, но не их моновалентные Fab-фрагменты способны активировать Рц.
Необходимость димеризации
Мутация, блокирующая димеризацию этого Рц, подавляет и его активацию лигандом. Лиганды обычно стимулируют олигомеризацию собственных Рц. Димеризация Рц может быть и конститутивной, т.е. не зависящей от лиганда (например, в случае сенсора кальция).
Необходимость димеризации для активации Рц, по-видимому, не является универсальным правилом. Например, степень димеризации Рц 8 опиоидов и олигомеризации Рц ТТГ снижается в присутствии агониста. Определённую роль в проведении сигнала может играть гетеродимеризация между близкородственными Рц. Так, Рц ГАМК (GABAB Pv2) способствует созреванию формы Рц GABAB R1 за счёт образования с ним гетеродимеров. Гетеродимер из опи-оидных Рц 5 и к приобретает свойства, отличные от свойств составляющих его Рц. Гетеродимеризация Рц соматостатина sst2A и sst3 ведёт к инактивации sst3 при одновременном снижении скорости десенситизации sst2A. Аналогичную супрессорную функцию выполняет Рц ангиотензина 2 по отношению к партнёру по гетеро-димеризации — Рц ангиотензина 1. В то же время образование димеров между sst2A и ц-Рц опиоидов не влияет на способность этих Рц связывать лиганды и проводить сигнал. Однако лиганд sst2A индуцирует фосфорилирование, интернализацию и десенситизацию не только своего Рц, но и партнёра по гетеродимеризации. Практически симметрично действует лиганд ц-Рц опиоидов. Ещё один тип последствий наблюдается при гетероолигомеризации Рц соматостатина sst5 и Рц дофамина D2R. Такой олигомер оказывается функционально более активным, чем его составляющие.
Таким образом, гомо- и олигомеризация Рц данного класса может иметь разные последствия для проведения гормональных сигналов. Обнаружена и патогенетическая роль гетеродимеризации: при преэклампсии резко увеличивается образование гетеродимеров между Рц ангиотензина 1 для вазоконстриктора ангиотензина II и Рц В(2) для вазорелаксанта брадикинина; такие гетеродимеры обеспечивают гиперчувствительность к гипертензивному действию ангиотензина, усугубляя развитие заболевания.
- Предыдущие статьи из рубрики: Эндокринология